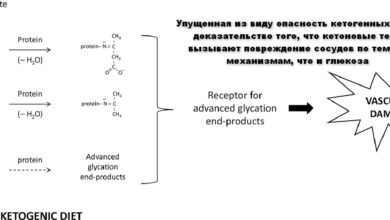
Кетоновые тала как онкометаболиты: для тех, кто до сих пор уверен, что рак питается исключительно глюкозой
Использование кетонового тела стимулирует рост опухоли и метастазирование (ссылка)
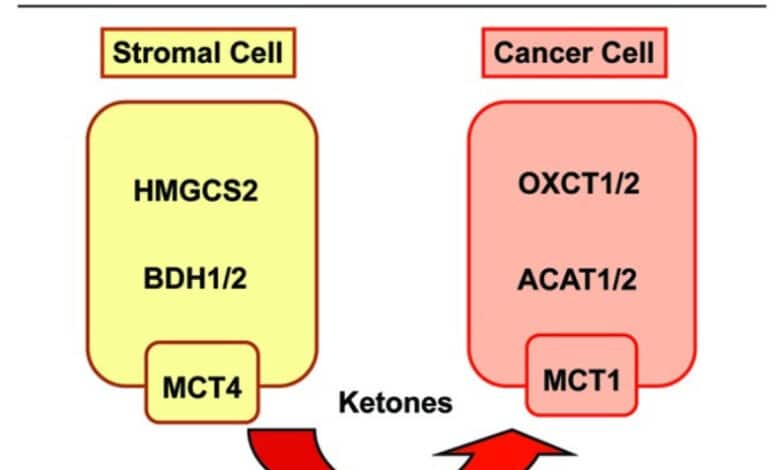
Недавно мы предоставили доказательства того, что опухоли человека могут иметь тот же тип метаболических проводников, что и мозг. Вкратце, мы предположили, что катаболические фибробласты с митохондриальной дисфункцией продуцируют кетоновые тела в строме опухоли. 4 , 5 Затем эти кетоновые тела повторно используются соседними раковыми клетками, которые перерабатывают эти кетоновые тела в качестве митохондриального топлива для окислительного фосфорилирования (OXPHOS), чтобы стимулировать анаболический рост опухоли.
Ранее мы предположили, что катаболические фибробласты генерируют митохондриальное топливо (например, кетоновые тела) для содействия анаболическому росту раковых клеток человека и их метастазированию. Мы назвали эту новую парадигму “метаболизмом опухоли two-compartment”. Здесь мы дополнительно проверили эту гипотезу, используя генетический подход.
Для этой цели мы сгенерировали hTERT-иммортализованные фибробласты, сверхэкспрессирующие ферменты, ограничивающие скорость выработки кетонов, а именно BDH1 и HMGCS2. Аналогичным образом, мы сгенерировали клетки рака молочной железы человека MDA-MB-231, сверхэкспрессирующие ключевые ферменты, которые позволяют повторно использовать кетоновые тела, OXCT1/2 и ACAT1/2. Интересно, что наши результаты непосредственно показывают, что кетогенные фибробласты являются катаболическими и подвергаются аутофагии с потерей экспрессии белка кавеолина-1 (Cav-1).
Кроме того, кетогенные фибробласты увеличивают массу митохондрий и рост соседних клеток рака молочной железы. Однако, что наиболее важно, кетогенные фибробласты также эффективно способствуют росту опухоли, без значительного увеличения ангиогенеза опухоли. Наконец, клетки MDA-MB-231, сверхэкспрессирующие ферменты, необходимые для повторного использования кетонов, демонстрируют резкое увеличение роста опухоли и метастатической способности.
Наши данные дают необходимые генетические доказательства того, что выработка и повторное использование кетоновых тел приводят к прогрессированию опухоли и метастазированию. Таким образом, ингибиторы кетонов должны быть разработаны в качестве новых терапевтических средств для эффективного лечения пациентов с прогрессирующим раком, рецидивом опухоли и метастатическим заболеванием. Таким образом, кетоновые тела ведут себя как онко-метаболиты, и мы непосредственно показываем, что ферменты HMGCS2, ACAT1/2 и OXCT1/2 являются истинными метаболическими онкогенами.
Чтобы предотвратить эту форму «двухкомпонентного метаболизма опухоли», следует разработать ингибиторы кетонов, чтобы остановить производство кетоновых тел в связанных с раком фибробластах и повторное использование кетоновых тел в эпителиальных раковых клетках. Эта простая стратегия может эффективно уморить раковые клетки голодом, «отключив их подачу топлива».