Исследования показывают, что вакцина Pfizer-BioNTech COVID-19 перепрограммирует врожденный иммунный ответ

Исследователи из Нидерландов и Германии предупредили, что вакцина Pfizer-BioNTech от коронавирусной болезни 2019 (COVID-19) вызывает сложное перепрограммирование врожденных иммунных ответов, что следует учитывать при разработке и использовании вакцин на основе мРНК.
Хорхе Домингес-Андрес и его коллеги говорят, что, хотя было доказано, что вакцина на 95% эффективна в предотвращении заражения тяжелым острым респираторным синдромом, вызванным коронавирусом 2 (SARS-CoV-2) и последующим COVID-19, мало что известно о широком распространении влияние вакцины на врожденный и адаптивный иммунные реакции.
В текущем исследовании ( не рецензируемом * ) исследовательская группа из Медицинского центра Университета Радбауд и Erasmus MC в Нидерландах, а также Центра исследований инфекций им. Гельмгольца (HZI), Ганноверской медицинской школы (MHH) и Университета им. Бонн, Германия, подтвердил эффективность вакцинации BNT162b2 в индукции эффективного гуморального и клеточного иммунитета против нескольких вариантов SARS-CoV-2.
Однако они также показали, что вакцина изменяет выработку воспалительных цитокинов клетками врожденного иммунитета после стимуляции как специфическими (SARS-CoV-2), так и неспецифическими (вирусными, грибковыми и бактериальными) стимулами.
После вакцинации у клеток врожденного иммунитета наблюдался пониженный ответ на toll-подобный рецептор 4 (TLR4), TLR7 и TLR8 — все лиганды, которые играют важную роль в иммунном ответе на вирусную инфекцию.
Нета и его коллеги также обнаружили, что цитокиновый ответ на грибки усиливался после вакцинации.
Предварительная версия исследования доступна на сервере medRxiv *. Препринт — это версия научной или научной статьи, которая предшествует официальному рецензированию и публикации в рецензируемом научном или научном журнале.
Ускоренное развитие новых вакцинных технологий
С тех пор, как в конце декабря 2019 года началась пандемия COVID-19, исследователи по всему миру спешат разработать вакцины, которые помогут бороться с глобальным кризисом в области здравоохранения.
Масштаб пандемии привел к ускоренной разработке новых вакцин на основе мРНК, первой из которых была зарегистрирована вакцина BNT162b2 от Pfizer-BioNTech.
Эта вакцина основана на рецептуре липидных наночастиц, модифицированной нуклеозидами мРНК, которая кодирует спайковый белок штамма SARS-CoV-2, который был выделен на ранней стадии пандемии в Ухане, Китай.
Белок-спайк является основной структурой, которую вирус использует для заражения клеток-хозяев, а его рецептор-связывающий домен (RBD) является основной мишенью для нейтрализующих антител после естественной инфекции или вакцинации.
Несколько испытаний фазы 3 показали, что BNT162b2 вызывает широкие гуморальные (антитела) и клеточные ответы, которые защищают от COVID-19. Тем не менее, многие проблемы остаются, пока эта и другие вакцины на основе мРНК внедряются во всем мире, при этом появление новых вариантов вызывает особую озабоченность.
Варианты, появившиеся в Великобритании (линия B.1.1.7), Южной Африке (B.1.351) и Бразилии (P.1), содержат множественные мутации в спайке, которые могут повлиять на тяжесть заболевания, вирусную передачу и эффективность вакцины. .
Кроме того, неизученной областью является вопрос о том, оказывает ли вакцинация BNT162b2 долгосрочное влияние на врожденные иммунные реакции:
Что сделали исследователи?
Исследователи показали, что одна доза вакцины BNT162b2 индуцирует высокие концентрации антител против спайков и против спайков RBD, а вторая доза через три недели вызывает еще более высокие уровни.
Все испытанные образцы сыворотки после вакцинации эффективно нейтрализовали вариант B.1.1.7, но 37,5% показали снижение нейтрализующей активности против варианта B.1.351.
А как насчет клеточного ответа?
Сообщалось, что вакцинация BNT162b2 активирует SARS-CoV-2-специфические CD4 + и CD8 + Т-клетки и увеличивает продукцию иммуномодулирующих цитокинов, таких как интерферон-γ (IFN-γ).
Таким образом, Домингес-Андрес и его коллеги оценили секрецию IFN-γ мононуклеарными клетками периферической крови (PBMC) в ответ на различные штаммы SARS-CoV-2 до и после вакцинации BNT162b2.
Вакцинация увеличила продукцию IFN-γ как минимум на 50% в 37,5% образцов, стимулированных стандартным штаммом SARS-CoV-2, в 50% образцов, стимулированных вариантом B.1.1.7 или B.1.351, но только в 18,8%. образцов, стимулированных баварским вариантом.
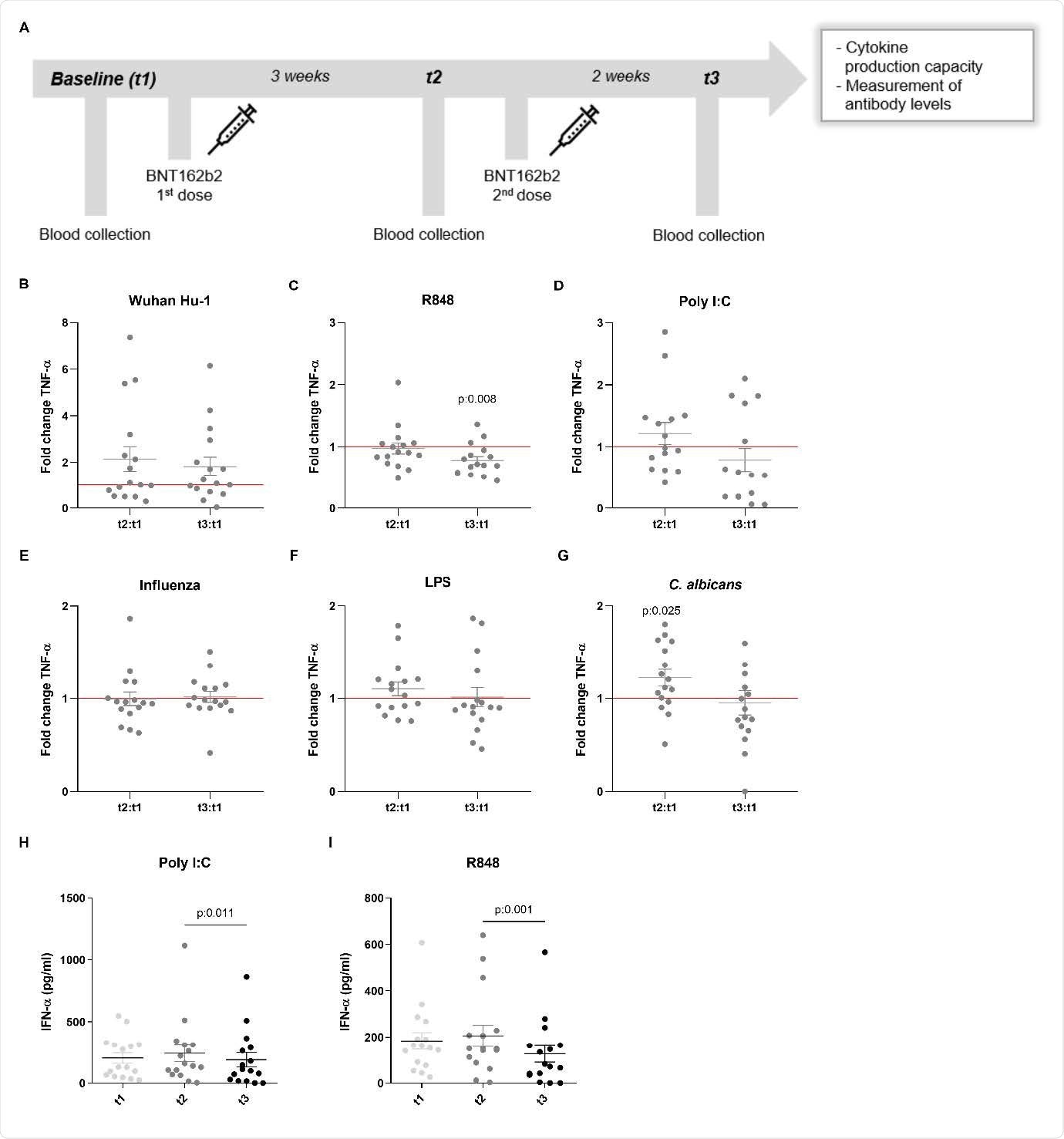
Цитокиновые ответы на определенные раздражители были снижены после вакцинации.
Интересно, что вакцинация BNT162b2 снижает продукцию IFN-γ после стимуляции TLR7 и агонистом TLR8 R848. Лиганды TLR7 и TLR8 играют ключевую роль в иммунном ответе на вирусную инфекцию.
Вакцинация также снижает выработку провоспалительных цитокинов, фактора некроза опухолей-α и интерлейкина-1β после стимуляции либо стандартным штаммом SARS-CoV-2, либо различными лигандами Toll-подобных рецепторов.
Напротив, ответы на грибковый патоген Candida albicans были выше после вакцинации.
Кроме того, продукция противовоспалительного цитокина интерлейкина-1Ra была снижена в ответ на Toll-подобный рецептор 4 и C. albicans . Это также предполагает сдвиг в сторону усиления воспалительной реакции на грибки после вакцинации, говорят исследователи.
Что советуют авторы?
Исследователи говорят, что в сочетании с сильными адаптивными иммунными ответами перепрограммирование врожденных ответов может способствовать либо более сбалансированной воспалительной реакции на инфекцию SARS-CoV-2, либо ослаблению врожденного иммунного ответа.
Влияние вакцинации BNT162b2 на врожденный иммунный ответ также может повлиять на реакцию на другие вакцинации, добавляет команда.
* Важное замечание
medRxiv публикует предварительные научные отчеты, которые не рецензируются и, следовательно, не должны рассматриваться как окончательные, руководящие в клинической практике / поведении, связанном со здоровьем, или рассматриваться как установленная информация.
- Домингес-Андрес Дж. И др. Вакцина мРНК BNT162b2 против SARS-CoV-2 перепрограммирует как адаптивные, так и врожденные иммунные ответы. medRxiv, 2021. doi: https://doi.org/10.1101/2021.05.03.21256520 , https://www.medrxiv.org/content/10.1101/2021.05.03.21256520v1









